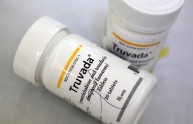
Si chiama Truvada ed è il primo primo farmaco approvato dall’americana Food and Drug Administration (FDA) per la prevenzione dell’infezione da HIV-1 per adulti non infetti, ma ad alto rischio di contagio. Il medicinale, a base di emtricitabina e tenofovir disoproxil fumarato, era stato già approvato dalla commissione degli esperti a maggio 2012 e oggi ha ottenuto il definitivo via libera alla commercializzazione con la nuova indicazione della “profilassi pre-esposizione” (PREP). Infatti il Truvada era già utilizzato come farmaco per la terapia in adulti e bambini affetti da HIV, associato ad altri agenti antiretrovirali.
Per una corretta e sicura prevenzione, essendone stata dimostrata l’efficacia solo nel 75% dei casi, il farmaco andrà assunto quotidianamente e sempre in combinazione con pratiche sessuali sicure, garantite dall’uso del profilattico.
Suscita infatti timore il fatto che l’approvazione di questo farmaco PREP, possa indurre alcuni soggetti ad una attività sessuale non protetta e quindi più a rischio.
Gli Stati Uniti in particolare hanno già da tempo avviato una grande campagna di informazione e prevenzione, attuata tra l’altro anche con la diffusione di test per l’HIV gratuiti da fare in farmacia o a casa, grazie ai kit domestici.
Secondo le indicazioni della casa farmaceutica produttrice Gilead Sciences, il Truvada PREP va assunto esclusivamente da persone risultate sieronegative al test per l’AIDS, che va effettuato immediatamente prima dell’inizio della terapia. Inoltre gli esami di screening per l’HIV-1 vanno ripetuti almeno a cadenza trimestrale.
L’assunzione del farmaco in soggetti risultati sieropositivi o che si sospetta siano affetti da infezione acuta da HIV non rilevata, viene fermamente sconsigliato dalla FDA, a causa del rischio che si tramuti in un ceppo più resistente.
Per quanto riguarda gli eventuali effetti collaterali, non ve ne sono di nuovi rispetto a quelli già noti, che sono: nausea, diarrea, dolore addominale, cefalea e perdita di peso. prima dell’assunzione, occorre verificare
L’approvazione definitiva del Truvada rappresenta dunque un importante progresso nella lotta all’epidemia dell’HIV, e si prevede che sarà l’argomento principe della Conferenza Internazionale sull’AIDS/HIV, che avrà luogo domenica 22 luglio 2012 a Washington.